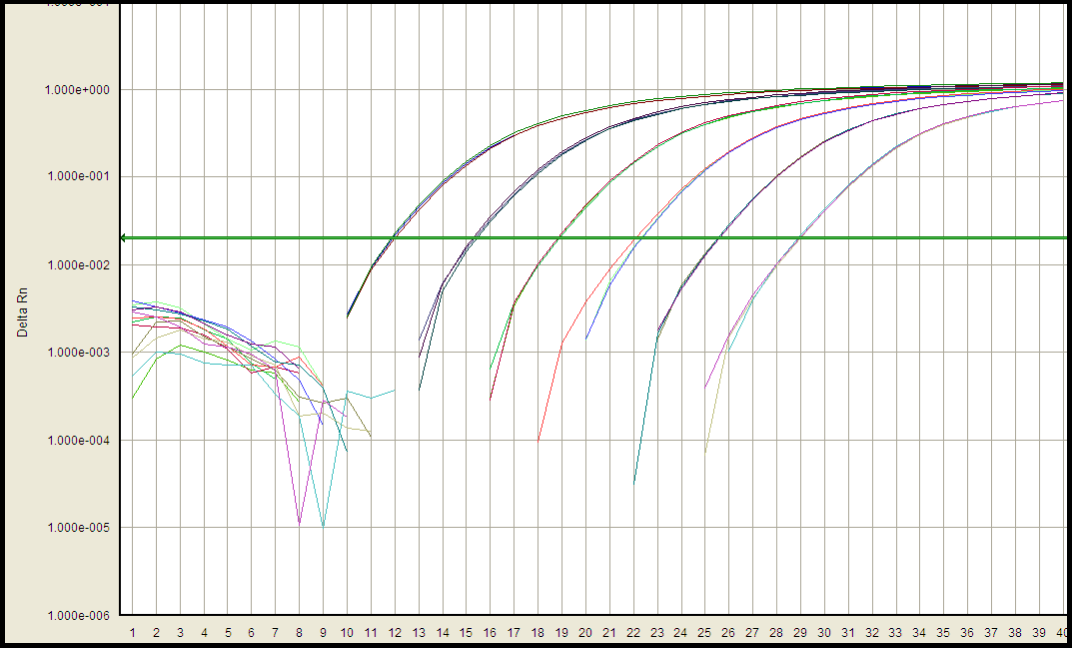
يتم التعبير عن المواد البيولوجية من مضيفات البكتيريا والخميرة والخلايا الحيوانية وخطوط الخلايا المستمرة. بما أن المنتجات البيولوجية يتم إنتاجها من ركيزة الخلية ، فمن المحتم أن يكون الحمض النووي المتبقي للخلية المضيفة موجودًا في المنتجات النهائية. لديها مخاطر محتملة من المناعة ، والأورام ، والعدوى بسبب الورم أو الجينات المرتبطة بالفيروسات في خطوط الخلايا المارة. يحتوي الحمض النووي المتبقي على مخاطر عالية محتملة للسلامة ويعتبر سمة جودة حرجة. الوكالات الحالية بما في ذلك ، الاتحاد الأوروبي ، وFDA كميات مقبولة من DNA المتبقية (أقل من 10 نانوغرام أو pg/dose). من بين طرق الكشف عن الحمض النووي المتبقي ، يعتبر qPCR الأكثر عملية لقياس كمية الحمض النووي المتبقي بسبب حساسيته ودقته ودقته وتوفير الوقت.
بما أن rDNA يمكن أن يأتي من مجموعة واسعة من المضيفين ، فقد توجد rDNA بأحجام وأشكال مادية مختلفة ، قد تكون الحدود المختلفة لمحتوى الحمض النووي وحجمه مقبولة لدى الهيئات التنظيمية إذا كانت مدعومة بأدلة علمية وتقييم قوي للمخاطر. يمكن أن يكون مستوى مخلفات الحمض النووي للخلية المضيفة بمثابة مؤشر على اتساق المنتج ومراقبة الجودة. الكشف عن الحمض النووي المتبقي يضمن الاتساق بين دفعات الإنتاج ويوفر مرجعا لتقييم جودة المنتج.
لتحليل تركيز الحمض النووي للخلية المضيفة وتوزيع الحجم ، يتم أولاً استخراج كسور الحمض النووي من العينة لضمان الكشف بدون مركبات مثبطة من مصفوفة العينة. الفصل بين الخرز المغناطيسي هو التقنية الأكثر استخدامًا لهذا الغرض ، مما يتيح عمليات الاستخراج الآلية التي تزيد من الإنتاجية والدقة.
لتحديد كفاءة استخراج الحمض النووي للخلية المضيفة المتبقية ، تتم إضافة كمية معروفة من الحمض النووي المستهدف ("spike") إلى العينة قبل الاستخراج. من خلال مقارنة كمية الحمض النووي المقاسة بعد الاستخراج مع الكمية المسننة ، يمكن حساب كفاءة الاستخراج. ثم يتم استخدام قيمة الكفاءة هذه لتحديد الحمض النووي للخلية المضيفة المتبقية في العينة. يشير انخفاض كفاءة الاستخراج إلى وجود مركبات مثبطة مستخلصة مع الحمض النووي.
يتطلب تطوير طريقة كشف حساسة ومحددة للغاية لخلية الحمض النووي المضيفة باستخدام جهاز فحص الكلور في الوقت الفعلي تصميم تمهيدي دقيق وتحسين تفاعل الكلور. خصوصية وحساسية منفي الوقت الحقيقي بسيتتأثر بدرجة حرارة التلدين ، والوقت ، وتركيزات الكاتينات والبادئات في عازل التفاعل. يمكن أن يؤدي استهداف جين موجود في نسخ متعددة إلى زيادة حساسية الفحص.
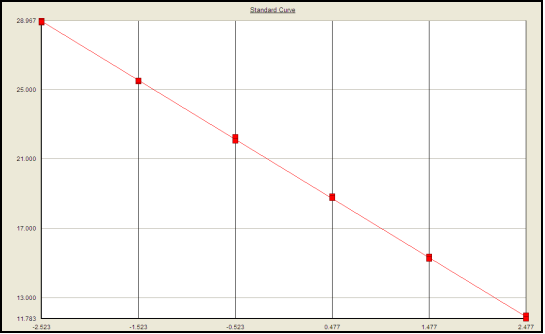
تم تقييم الخطوط ونطاق طرق الفحص عن طريق حساب خط الانحدار للمنحنى القياسي. تم تقييم الدقة من خلال تحليل النسبة المئوية للتعافي لمعايير الحمض النووي المسننة بثلاثة تركيزات مختلفة. تم تقييم دقة الفحص الداخلي والداخلي من خلال ٪ CV لجميع QCs في كل مستوى. تم تحديد الحساسية عن طريق فحص اللود واللوق. تم تقييم التخصيص من خلال تحليل عينات الحمض النووي أو مجموعة من الحمض النووي المصفوفة المستخرج من الأنواع/السلالة ذات الصلة. تم تقييم المتانة من خلال تقييم ثبات أداء الفحص في ظل ظروف تخزين مختلفة.
يشمل نطاق التحقق من صحة مقايسة الحمض النووي للخلية المضيفة المتبقية ما يلي:
الدقة
الدقة
خصوصية
الحد من الكمية (LOQ)
الخطية
النطاق
متانة
يسمح مقايسة تم التحقق منها بالكامل باستخدام المنتجات المتاحة تجاريًا أو مجموعات مصممة خصيصًا تستهدف تسلسل الحمض النووي للمضيف ، مما يجعلها قابلة للتطبيق للاختبار بين المنتجات البيولوجية.
دراسة حالة-كمية خلية مضيف متبقية من الحمض النووي
CHO HCD التحقق من الأداء-
كفاءة التضخيم القياسية: ency ، معامل الارتباط